Từ thực phẩm bảo vệ sức khỏe…
Hiện nay, chị em phụ nữ có nhu cầu sử dụng thực phẩm chức năng và thực phẩm bảo vệ sức khoẻ (TPBVSK) ngày càng cao. Trong bối cảnh thị trường có nhiều cạnh tranh, việc quảng cáo loại sản phẩm này của một số đơn vị đang tồn tại những bất cập.
Điều 27, Nghị định 115/2018/NĐ-CP quy định: Nội dung quảng cáo phải phù hợp với công dụng, tác dụng của sản phẩm đã được công bố trong bản công bố sản phẩm. Đối với thực phẩm bảo vệ sức khỏe: Phải có khuyến cáo “Thực phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh”. Ngoài ra, không được quảng cáo thực phẩm chức năng gây hiểu nhầm sản phẩm đó là thuốc (khoản 4, Điều 5, Nghị định 181/2013/NĐ-CP).
Tuy nhiên trên thực tế, nhiều loại TPBVSK vẫn đang được ngang nhiên “thổi phồng” công dụng “trị bách bệnh”.
Đơn cử như viên đặt phụ khoa Nữ Oa sản xuất tại công ty TNHH Ngân Kiều Pharma (MST: 2400818731, số 02, ngõ 122, Hà Vị 1, phường Thọ Xương, thành phố Bắc Giang, tỉnh Bắc Giang), phân phối bởi công ty Cổ phần Đông dược Vũ Đức (theo thông tin trên bao bì) - MST: 0315416019 ĐKKD: 496/63/19A1 Dương Quảng Hàm, phường 6, quận Gò Vấp, TP.Hồ Chí Minh; trụ sở: 28 đường số 2, KDC Cityland, phường 7, quận Gò Vấp.
Cụ thể, PV ghi nhận trên nhiều website như “dongduocvuduc.net”, “netdep.com.vn”, “phukhoanuoa.net”... viên đặt phụ khoa Nữ Oa được quảng cáo với những công dụng như: “khắc phục” và “điều trị” nhiều chứng bệnh phụ khoa. Ngoài ra, một số trang web còn sử dụng hình ảnh bác sĩ, dược sĩ để quảng cáo sản phẩm.

Quảng cáo tràn lan viên đặt phụ khoa Nữ Oa có tác dụng như thuốc chữa bệnh.
Đặc biệt, trang web “dongduocvuduc.net” còn nêu rõ, sản phẩm có khả năng hỗ trợ chữa trị các bệnh về răng miệng. Từ số hotline 096160XXXX hiển thị trên trang web này, PV đã được nhân viên giới thiệu một số thông tin qua tài khoản Zalo. Cụ thể, khi PV hỏi về công dụng, nhân viên tư vấn cho biết: “Người lớn, trẻ em khi ngậm viên đặt phụ khoa từ 1-2 lần/ngày sẽ chữa được sâu răng”.
Đồng thời, nhân viên đưa ra 2 giấy tiếp nhận đăng ký bản công bố số 1100/2019/ĐKSP và số 7137/2019/ĐKSP, cấp bởi cục An toàn thực phẩm - bộ Y tế, có cùng tên “THỰC PHẨM BẢO VỆ SỨC KHỎE VIÊN HOÀN NỮ OA”, sử dụng bằng cách ngậm; uống từ 4-6 viên một ngày.
Đáng nói, hai bản công bố kể trên đều không có lưu ý, hướng dẫn cách đặt vào âm đạo như thế nào; đồng thời khác nhau hoàn toàn về nội dung (công bố số 1100/2019/ĐKSP có đối tượng sử dụng là người bị viêm niêm mạc miệng, viêm lợi, còn công bố số 7137/2019/ĐKSP đối tượng sử dụng dành cho phụ nữ bị khí hư, bạch đới).

Hình ảnh 2 phiếu xác nhận nội dung quảng cáo của TPBVSK Viên hoàn Nữ Oa với công dụng hoàn toàn khác nhau.
Để kiểm chứng, ngày 9/5/2023, PV tiếp tục liên hệ qua số hotline như đã đề cập và đặt mua bộ sản phẩm viên đặt phụ khoa Nữ Oa với giá 649.000 đồng. Bộ phận bán hàng khẳng định “viên đặt Nữ Oa là thuốc đông y đăng ký trên giấy tờ dưới dạng thực phẩm chức năng” và cho biết viên đặt hay viên hoàn đều là một.
Sau khoảng 6 ngày chờ đợi, PV đã nhận được “hàng ship”. Trên tay PV lúc này là hộp sản phẩm viên đặt phụ khoa Nữ Oa. Theo quan sát thực tế, không có bất cứ hướng dẫn nào theo dạng uống; ngậm như 2 bản công bố mà website đăng tải. Công dụng tuyệt nhiên không đề cập đến khả năng hỗ trợ điều trị bệnh răng miệng giống với quảng cáo.
Trả lời tạp chí Đời sống và Pháp luật, cục An toàn thực phẩm xác nhận cấp 02 giấy tiếp nhận đăng ký bản công bố sản phẩm số 1100/2019/ĐKSP ngày 28/01/2019 và số 7137/2019/ĐKSP ngày 17/06/2019 cho sản phẩm thực phẩm bảo vệ sức khoẻ VIÊN HOÀN NỮ OA lần lượt do công ty TNHH sản xuất thương mại Thiên Ân Dược và công ty CP Đông dược Vũ Đức công bố và chịu trách nhiệm sản phẩm. Cục An toàn thực phẩm khẳng định, không cấp giấy tiếp nhận đăng ký công bố sản phẩm VIÊN ĐẶT PHỤ KHOA NỮ OA.
Phía Cục đang xác minh, làm rõ những dấu hiệu vi phạm về quảng cáo , trong trường hợp xác định có vi phạm sẽ xử lý nghiêm và công khai kết quả xử lý theo quy định. Đồng thời, khuyến cáo người tiêu dùng cần cẩn trọng trước những chiêu trò và các sản phẩm thực phẩm bảo vệ sức khoẻ nói trên, tránh “tiền mất tật mang”.

Số công bố thể hiện viên đặt phụ khoa Nữ Oa là TTBYT loại B. Công dụng tuyệt nhiên không đề cập đến khả năng hỗ trợ điều trị bệnh răng miệng như quảng cáo.
…Đến trang thiết bị y tế loại A, B
Theo tìm hiểu của PV, trước đây viên đặt phụ khoa Nữ Oa đã từng được công bố là TTBYT loại A do công ty Vũ Đức là chủ sở hữu và chịu trách nhiệm phân phối, được công ty Lasva sản xuất.
Từ tháng 7/2020, công ty Lasva ngừng thực hiện gia công sản phẩm trên do không phù hợp là thiết bị y tế theo Công văn 3453/BYT-TB-CT của bộ Y tế (tuy nhiên, hiện tại, phiếu công bố TTBYT loại A này vẫn còn tồn tại trên cổng thông tin sở Y tế TP.HCM).

Đến ngày 2/7/2021, viên đặt phụ khoa Nữ Oa tiếp tục “khoác áo” TTBYT loại A do công ty Ngân Kiều Pharma công bố và đã được ông Nguyễn Văn Bình, Phó Giám đốc sở Y tế Bắc Giang ký giấy tiếp nhận. Nhưng chỉ trong thời gian ngắn (khoảng 20 ngày, tức vào 21/7/2021 – PV), “chiếc áo” này đã “bị” chính vị Phó Giám đốc Nguyễn Văn Bình “cởi bỏ” bằng quyết định thu hồi hồ sơ công bố do chính tay mình ký tiếp nhận.
Đến ngày 22/1/2022 (6 tháng sau), viên đặt Nữ Oa Vũ Đức lại được khoác lên mình một “tấm áo mới” là TTBYT loại B, vẫn do công ty Ngân Kiều công bố và sản xuất (công bố số 220000005/PCBB-BG).
Trong công bố này, căn cứ để phân loại theo mức độ rủi ro là theo Quy tắc 5, phần B của Thông tư 39/2016/TT-BYT. Tuy nhiên, theo tìm hiểu của PV, Thông tư 39/2016/TT-BYT đã hết hiệu lực kể từ ngày 01/01/2022. Cụ thể, ngày 1/8/2022, bộ Y tế ra Thông tư số 05/2022/ TT-BYT quy định chi tiết thi hành một số điều của Nghị định số 98/2021/NĐ-CP ngày 8/11/2021 của Chính phủ về Quản lý trang thiết bị y tế. Tại khoản 4, Điều 7, Thông tư 05 nêu rõ các văn bản hết hiệu lực thi hành, trong đó có Thông tư 39/2016/TT-BYT.
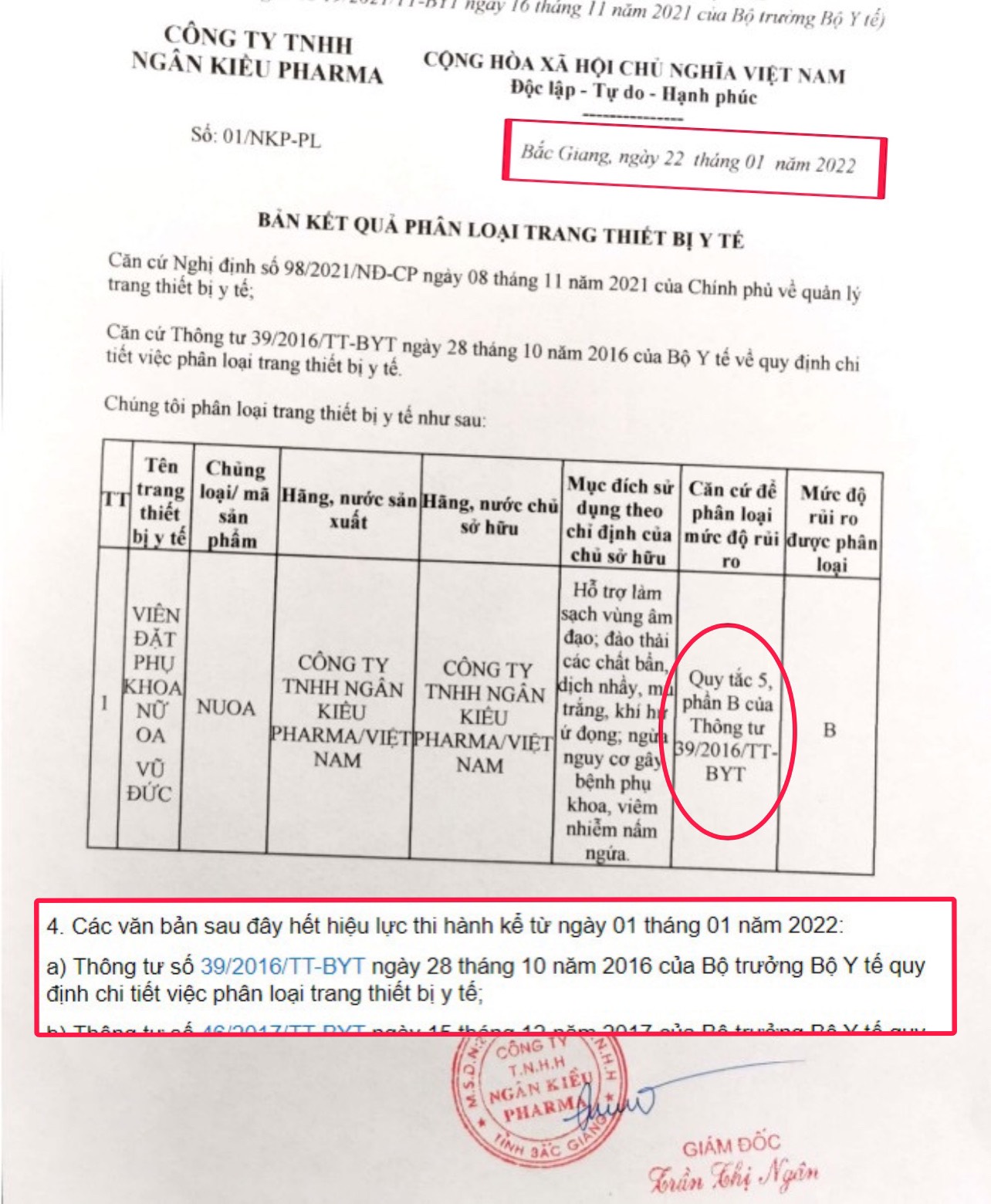
Hình ảnh phiếu công bố TTBYT loại B trên cổng thông tin bộ Y tế.

Khi tra cứu số 220000005/PCBB-BG trên cổng thông tin điện tử của bộ Y tế, PV nhận được kết quả là văn bản công bố của công ty TNHH Ngân Kiều Pharma đề ngày 27/1/2022 có nội dung nêu rõ: “Viên đặt phụ khoa Nữ Oa Vũ Đức là TTBYT loại B; Quy cách đóng gói (nếu có): Hộp 5 viên, hộp 10 viên”.
Tuy nhiên, bộ sản phẩm PV đã mua dù trùng khớp với số công bố này nhưng thực tế bên trong lại là loại 06 viên hoàn, 06 cốt xông rửa.
Một điểm đáng chú ý nữa, viên đặt phụ khoa có thể không phù hợp định nghĩa TTBYT (cần rà soát thành phần hoạt chất, cơ chế hoạt động của sản phẩm và quy tắc phân loại TTBYT) theo Công văn số 2098/BYT-TB-CT của bộ Y tế ngày 12/04/2023 (mục 3, phần II và mục 11 phần I).

Danh sách đi kèm Công văn số 2098/BYT-TB-CT.
Để tìm hiểu rõ hơn về sản phẩm này, PV đã đến cơ sở sản xuất của công ty TNHH Ngân Kiều Pharma (địa chỉ: tổ dân phố Ngoài Hạ, thị trấn Cao Thượng, huyện Tân Yên, tỉnh Bắc Giang).
Tại địa chỉ trên, bà Ngân (Giám đốc công ty Ngân Kiều) cho biết: “Từ khi có công văn, bên tôi không sản xuất nữa mà chỉ sản xuất các đơn đã đặt trước đó và cũng dừng hẳn từ Tết (2023) đến nay”.
Vậy, sản phẩm này bản chất là gì? Để giúp bài viết có thêm tính khách quan, thông tin đa chiều, PV đã liên hệ tới sở Y tế tỉnh Bắc Giang nhưng không nhận được phản hồi.
PV cũng đã đã gửi câu hỏi tới vụ Trang thiết bị và Công trình y tế, đại diện đơn vị này cho biết hồ sơ công bố do công ty sản xuất tự công bố, sở Y tế Bắc Giang quản lý.

Cần rà soát lại hồ sơ công bố sản phẩm
Liên quan đến nội dung này, trao đổi với PV, luật sư Nguyễn Công Tín - công ty Luật FDVN, đoàn Luật sư thành phố Đà Nẵng cho rằng: “Việc quảng cáo viên đặt phụ khoa Nữ Oa (giấy phép quảng cáo là Thực phẩm bảo vệ sức khoẻ) có tác dụng như thuốc chữa bệnh; sử dụng hình ảnh bác sĩ, dược sĩ như phản ánh của PV là không phù hợp với quy định của pháp luật (căn cứ Điều 27, Nghị định 15/2018/NĐ-CP và Điều 5, Nghị định 181/2013/NĐ-CP). Theo chế tài xử phạt hành chính tối đa lên đến 30.000.000 đồng.
Trường hợp viên đặt phụ khoa Nữ Oa công bố tiêu chuẩn sản xuất cho sản phẩm hộp 05 và 10 viên đặt. Bộ sản phẩm PV đã mua dù trùng khớp với số công bố nhưng thực tế bên trong lại là loại 6 viên hoàn, 6 cốt xông rửa. Như vậy, rõ ràng công ty TNHH Ngân Kiều (đơn vị sản xuất) đã sản xuất không đúng với bản công bố sản phẩm.
Nếu công ty Ngân Kiều không thực hiện đăng ký lại bản công bố sản phẩm theo quy định của pháp luật (trong trường hợp có sự thay đổi thành phần cấu tạo) hoặc không thực hiện thông báo bằng văn bản về nội dung thay đổi sau công bố đến cơ quan Nhà nước có thẩm quyền thì có thể bị xử phạt từ 40 triệu đồng đến 60 triệu đồng (điểm a, b khoản 4, Điều 22, khoản 2, Điều 3 Nghị định 115/2018/NĐ-CP, được sửa đổi bổ sung bởi Nghị định 124/2021/NĐ-CP).
Ngoài ra hình thức xử phạt bổ sung là tước quyền sử dụng Giấy tiếp nhận đăng ký bản công bố sản phẩm từ 10 tháng đến 12 tháng.
Liên quan đến thông tin viên đặt phụ khoa Nữ Oa phân loại là TTBYT loại B có phù hợp hay không, luật sư Tín đưa ra quan điểm: “Viên đặt phụ khoa Nữ Oa được quảng cáo với công dụng như "khắc phục" và "điều trị" nhiều chứng bệnh phụ khoa, chữa sâu răng, niêm mạc miệng, viêm lợi thì việc xếp nó là TTBYT theo tôi là chưa phù hợp.
Trên cơ sở thành phần, công dụng, cơ chế hoạt động của sản phẩm, các cơ quan chuyên môn về y tế cần phải xem xét, rà soát lại các hồ sơ công bố sản phẩm không phù hợp là TTBYT. Nếu có sai sót thì cần phải thu hồi, đính chính theo đúng quy định của pháp luật”.
Hương Thắm - Thạch Thảo